硅(Si)
硅,是一种化学元素,化学符号是Si,原子序数是14,属于元素周期表上IVA族的类金属元素。硅原子有四个外围电子,与同族的碳相比,硅的化学性质更为稳定。硅在宇宙中的储量排在第八位。硅以化合物形式存在于在地壳中,是含量仅次于氧的第二丰富元素。硅的应用领域广泛,从中国最早的陶瓷工艺到现代光纤通信、宇航、电子等领域都有硅材料的应用。 | 元素名称 | 硅 | 元素符号 | Si | 原子序数 | 14 | 相对原子质量
(12C=12.0000) | 28.0855 | | 英文名称 | Silicon | | 原子结构 | 原子半径(Å) | 1.46 | 原子体积(cm3/mol) | 12.10 | 电子模型 | 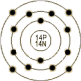
| | 电子构型 | 1s2 2S2P6 3S2P2 | 离子半径(Å) | 0.4 | | 共价半径(Å) | 1.11 | 氧化态 | 4 | | 发现 | 1824 在瑞典,斯德哥尔摩, 由 J.J. Berzelius 发现。 | | 命名起源 | from 'silicis' (Latin) - flint | | 来源 | 硅是第二个最丰富的元素,在地可中含25%,是构成粘土、沙、花岗岩和石英的主要成分。 | | 用途 | 用于制造玻璃,太阳能电池,水泥和半导体等等。 | | 物理性质 | 状态 | 硬的深灰色非金属 | 熔 点(℃) | 1410 | 沸 点(℃) | 2355 | | 密度(g/cc,300K) | 2.33 | 比 热(J/gK) | 0.71 | 蒸发热(KJ/mol) | 384.22 | | 熔化热(KJ/mol) | 50.55 | 导电率(106/cm) | 2.52E-12 | 导热系数(W/cmK) | 1.48 | | 自燃点(℃) | | 闪 点(℃) | | | | | 化学性质 | | | 地质数据 | 丰 度 | | 滞留时间(年) | 30000 | 太阳
(相对于 H=1×1012) | 4.47×107 | | 海水中(ppm) | - | 地壳(ppm) | 277100 | 大西洋表面 | 0.03 | | 太平洋表面 | 0.03 | 大气(ppm(体积)) | - | 大西洋深处 | 0.82 | | 太平洋深处 | 4.09 | | | | | | 生物数据 | 人体中含量 | | 肝(ppm) | 12-120 | | 器官中 | | 肌肉(ppm) | 100-200 | | 血(mg dm-3) | 3.9 | 日摄入量(mg) | 18-1200 | | 骨(ppm) | 17 | 人(70Kg)均体内总量(mg) | 0.1 |
硅的同位素信息 | 同位素 | % | 质量 | 自旋 | 核磁矩 | 磁旋比 | Q | 频率 | 吸收率 | | 28 | 92.23 | 27.976926 | | | | | | | | 29 | 4.67 | 28.976497 | 1/2 | -0.96179 | -5.319 | 0 | 19.867187 | 3.68×10-4 | | 30 | 3.1 | 29.97377 | | | | | | | | [31] | 0 | 30.975363 | | | | | | | | [32] | 0 | 31.974148 | | | | | | |
| |
您可能感兴趣的产品:
|